2026年第一季度,国家市场监督管理总局食品审评中心(以下简称“审评中心”)持续深化保健食品审评审批全流程规范化建设,聚焦行业合规升级与高质量发展需求,实现审评意见出具、核查确认、批件发放等环节的精准衔接与高效运转,为保健食品行业年初发展奠定坚实监管基础。本动态基于审评中心公开的官方数据,从政策发布、审评意见发放、核查与批件发放等核心维度展开详细分析。
PART1 政策发布
第一季度,审评中心围绕行政许可全生命周期管理、注册现场核查效率提升等行业核心关切,发布2项关键政策文件,进一步完善保健食品监管流程,优化审批服务,防范行业合规风险,持续夯实行业高质量发展的制度保障,与去年第四季度备案管理、申报规范相关政策形成有效衔接,推动监管工作提质增效。
《关于对注册申请人注销的24件保健食品终止行政许可公告》(2026年1月22日发布):为规范保健食品行政许可管理,落实行政许可全生命周期监管要求,依法推进注销申请人相关保健食品行政许可终止工作,明确对注册申请人注销的24件保健食品依法终止行政许可,同步公开相关产品信息,清晰界定行政许可终止的适用情形与流程,既是对《保健食品注册与备案管理办法》中注销相关规定的具体落地,也有助于清理无效行政许可,节约监管资源,引导行业有序退出低效产品,推动行业资源优化配置,同时为市场主体提供明确的行政许可终止指引,降低行业合规风险。
《关于加快反馈保健食品注册现场核查有关信息的通知》(2026年3月16日发布):聚焦保健食品注册现场核查信息反馈不及时、流程衔接不畅等行业痛点,明确现场核查信息反馈的时限、内容、方式及责任主体,加快核查信息流转效率,推动核查环节与审评审批环节高效衔接,帮助企业及时掌握核查进展、梳理存在问题、优化应对方案,有效提升注册核查及后续审批效率,进一步规范注册核查全流程管理,保障保健食品注册审批工作顺畅推进,助力企业缩短注册周期、降低合规成本。
PART2 审评意见通知书发放
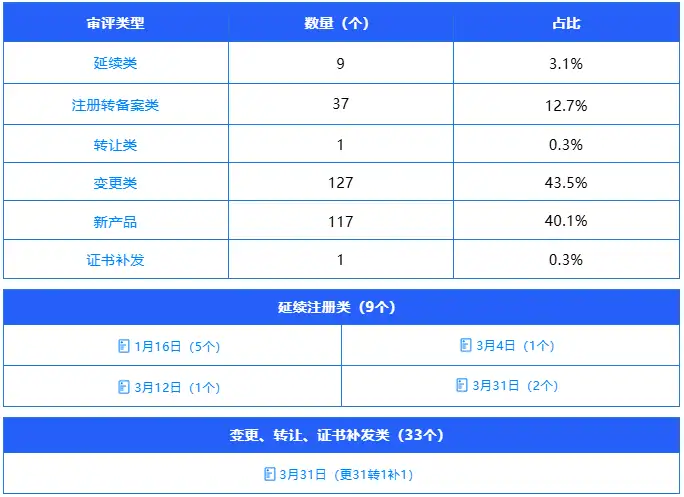
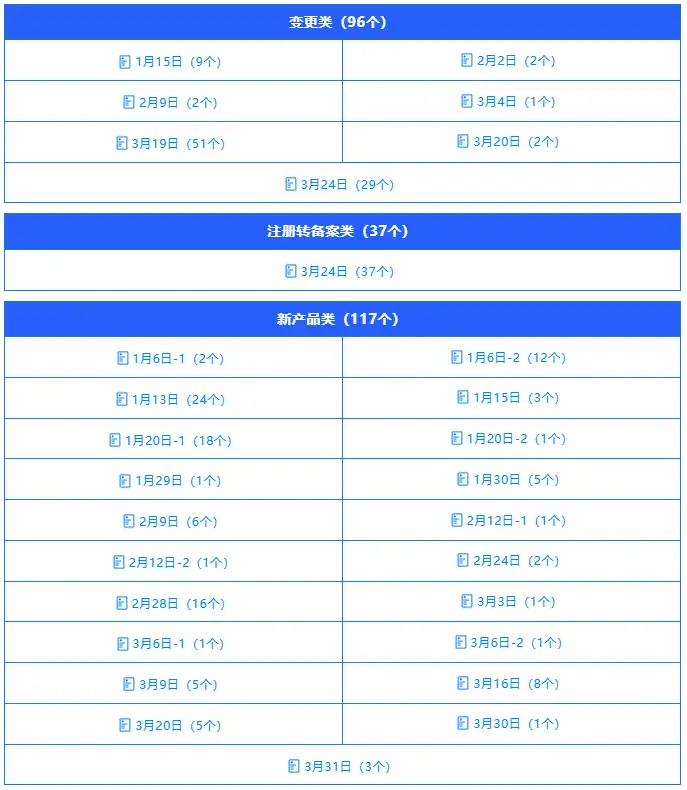
2026年第一季度,审评中心共发布保健食品审评意见通知书292个,较去年第四季度(765个)减少62%,审批节奏回归常态,行业需求结构较去年年末呈现颠覆性调整,与去年第四季度的需求特征形成鲜明反差,覆盖转让、延续、变更、注册转备案及新产品五大核心类别,具体数据及分析如下:
延续类:9个(占比3.1%),较去年第四季度(583个)减少98.5%,占比下降73.1个百分点,需求规模断崖式收缩。这一变化与去年第四季度“存量产品资质延续需求集中释放”形成强烈对比,核心原因在于年末集中完成延续申报后,第一季度行业进入延续需求淡季,多数企业已顺利完成产品资质衔接,仅少量特殊情形产品提交延续申请,完全符合行业周期性需求规律。
变更类:127个(占比43.5%),较去年第四季度(86个)增长47.7%,占比提升32.3个百分点,一跃成为本季度最核心的需求类别。变更需求主要集中在标签说明书合规优化、产品技术要求完善、生产场地及工艺调整等方面,相较于去年第四季度,企业合规管理更加常态化,主动适配监管政策更新、贴合消费市场需求升级的主动性进一步提升,成为推动变更需求逆势增长的核心动力。
注册转备案类:37个(占比12.7%),较去年第四季度(26个)增长42.3%,占比提升9.3个百分点。随着注册与备案双轨制的持续深化,原注册产品转备案工作在去年第四季度“平稳收尾”的基础上,本季度需求小幅回升,呈现常态化推进态势,行业产品管理体系进一步完善,转备案流程趋于顺畅高效,体现出双轨制运行的成熟度持续提升。
转让类:1个(占比0.3%),较去年第四季度(13个)减少92.3%,占比下降1.4个百分点,需求持续处于极低水平。与去年第四季度“资源整合节奏放缓”的态势相比,本季度企业资源整合意愿进一步降低,转让需求近乎停滞,主要受年初企业聚焦自身经营规划、暂缓资源调整的影响,符合行业年初稳扎稳打、聚焦核心业务的发展常规。
新产品:117个(占比40.1%),较去年第四季度(57个)大幅增长105.3%,占比提升32.6个百分点,与变更类并列成为本季度核心需求。这一变化延续并强化了去年第四季度新产品审评提速的良好态势,核心得益于审评中心持续优化新产品审评流程、清理积压任务的成效,本季度持续推进各类新产品审评工作,既彰显了审批效率的持续提升,也进一步激发了企业研发创新的积极性,推动行业新产品申报进入持续活跃阶段。
PART3 核查通知与批件发放
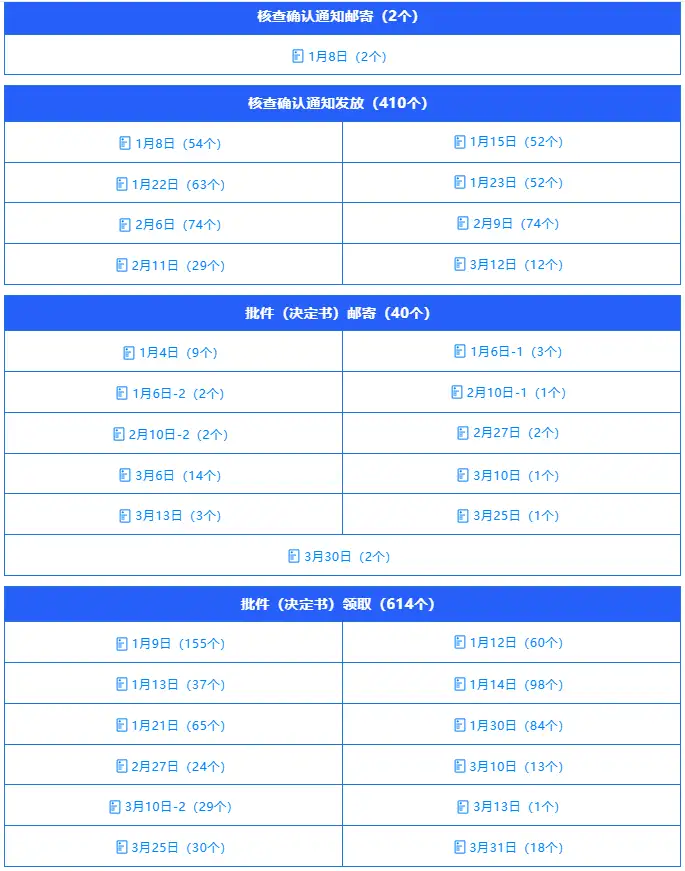
在审评意见出具的基础上,审评中心继续高效推进核查确认与批件发放环节,强化全流程闭环管理,确保审批结果及时落地。本季度共发送核查确认通知412个,完成批件(决定书)邮寄40个、通知领取614个,两类渠道合计覆盖654个审批事项。