2025年第三季度,国家市场监督管理总局食品审评中心(以下简称“审评中心”)稳步推进保健食品审评审批各项工作,从审评意见出具到核查确认、批件发放等全流程高效衔接,为保健食品行业规范发展提供了有力保障。本动态基于审评中心公开的官方数据,从政策发布、审评意见发放、核查与批件发放等维度展开详细分析。
PART1 政策发布
第三季度,审评中心围绕行业实操痛点与合规需求,密集发布3项关键政策文件,为企业办理相关业务提供明确指引。
《“双无” 保健食品换证常见问题及解答(第三批)》《“双无” 保健食品换证常见问题及解答(第四批)》:持续回应企业在 “双无” 保健食品换证过程中的高频疑问,进一步细化操作流程,降低企业合规成本。
《保健食品注册证书部分注册人注销变为单方持有技术转让办理指引》:针对注册人注销后证书单方持有场景下的技术转让业务,明确办理标准与流程,规范行业资源整合中的审批衔接。
PART2 审评意见通知书发放
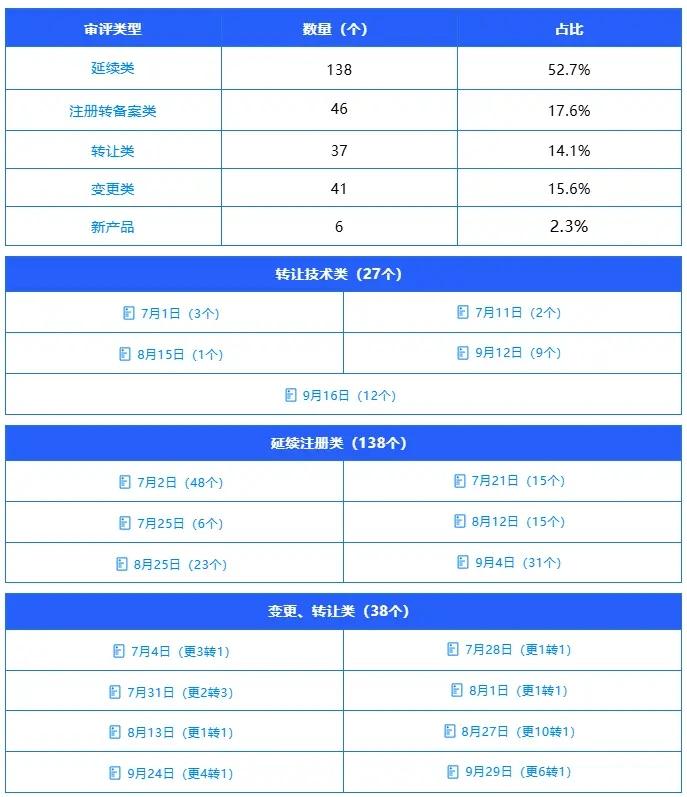
2025年第三季度国家市场监督管理总局食品审评中心共发布审评意见通知书262个,覆盖转让、延续、变更、注册转备案及新产品五大核心类别,具体数据及分析如下:
延续类:138个(占比52.7%),反映行业存量产品合规延续需求集中,也体现出审评中心对成熟产品合规性审核的高效把控。
注册转备案类:46个(占比17.6%),自保健食品注册与备案双轨制实施以来,注册转备案通道持续畅通,本季度的审批数据表明,符合备案条件的原注册产品正有序完成类别转换,行业产品管理体系进一步优化。
转让类:37个(占比14.1%),转让类审批活跃体现出保健食品行业资源整合步伐加快,部分企业通过产品转让实现资源优化配置。
变更类:41个(占比15.6%),变更类审批则主要集中在技术要求等方面,反映出企业根据市场需求和监管要求及时升级和规范产品的合规意识增强。
新产品:数量保持低位,凸显注册申报的科学性门槛,也反映出行业在新原料应用、功能声称创新等方面仍存在提升空间,未来需进一步激发企业研发创新活力。
PART3 核查通知与批件发放
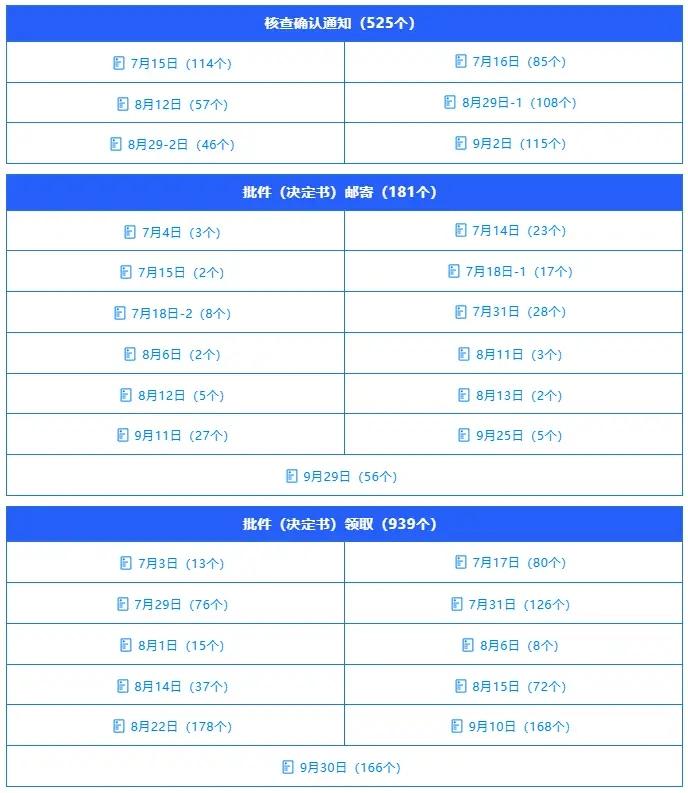
在审评意见出具的基础上,审评中心同步推进核查确认与批件发放等后续环节,保障审批流程闭环管理,各项工作指标均保持较高效率:本季度共邮寄核查确认通知 525 个,核查工作规模显著高于审评意见发放数量,凸显核查是本季度审评工作的核心重点,也体现出审评中心对产品真实性、合规性的核查力度持续加强;同时完成批件(决定书)邮寄 162 个、通知领取 939 个,两类批件流转渠道合计覆盖 1101 个审批事项。